
С.Л. Березина, В.Н. Горячева, Н.Н. Двуличанская
98
ISSN 1812-3368. Вестник МГТУ им. Н.Э. Баумана. Сер. Естественные науки. 2017. № 2
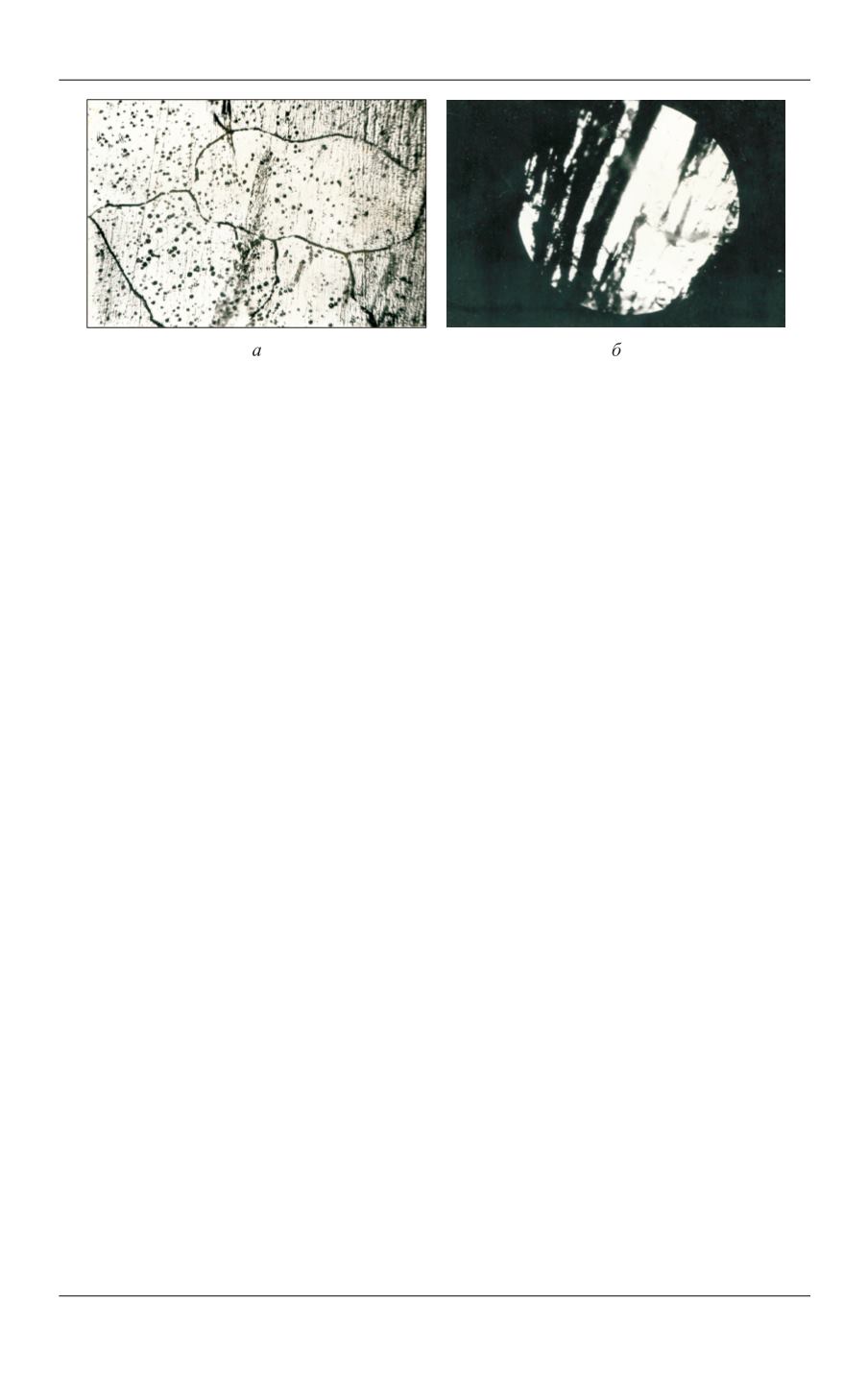
Рис. 1.
Исходная микроструктура (
а
) и микрофотография (
б
) поверхности сплава
W–Zr (18 %) в процессе анодного растворения
В зависимости от потенциала и рН раствора возможно образование кисло-
родных соединений вольфрама [5–7]:
+
2
2
W 2Н О = WО 4Н 4
е
+
2
2
2 5
2WО Н О = W О 2Н 2
е
+
2 5
2
3
W О Н О = 2WО 2Н 2
е
2
+
2
4
W 4Н О = WО 8Н 6
е
2
+
2
2
4
WО 2Н О = WО 4Н 2
e
2
+
2 5
2
4
W О 3Н О = 2WО 6Н 2
e
В области активного анодного растворения возможен разряд гидроксид-
ионов
2
2ОН = О Н O 2
е
образующийся атомарный кислород окисляет участки анода, свободные от пер-
вичной пассивирующей пленки, до высших оксидов
3
WО ,
частично раство-
ряющихся в щелочи с образованием устойчивых вольфраматов:
3
2
4
2
WО 2NaOH= Na WО Н O
Значения стационарных потенциалов
ст
в электролите 15 % NaOH + 5 % NaF
для образцов сплава с различным содержанием циркония приведены ниже. Увели-
чение содержания циркония в сплаве от 0,9 до 18 % оказывает активирующее
влияние, смещая значения потенциалов
ст
в область отрицательных значений.
По данным, приведенным в работе [7], присутствие в электролите фторид-ионов
способствует модификации сформированной на воздухе оксидной пленки цирко-
ния, разблагораживанию его электродного потенциала и активации анодного про-
цесса.
При анодной поляризации образцов наблюдались состояния активного
растворения, пассивации и глянцевания. Уменьшение анодной активности об-
разца в процессе анодного растворения связано с образованием на поверхности
неравномерной оксидной пленки [8].
















