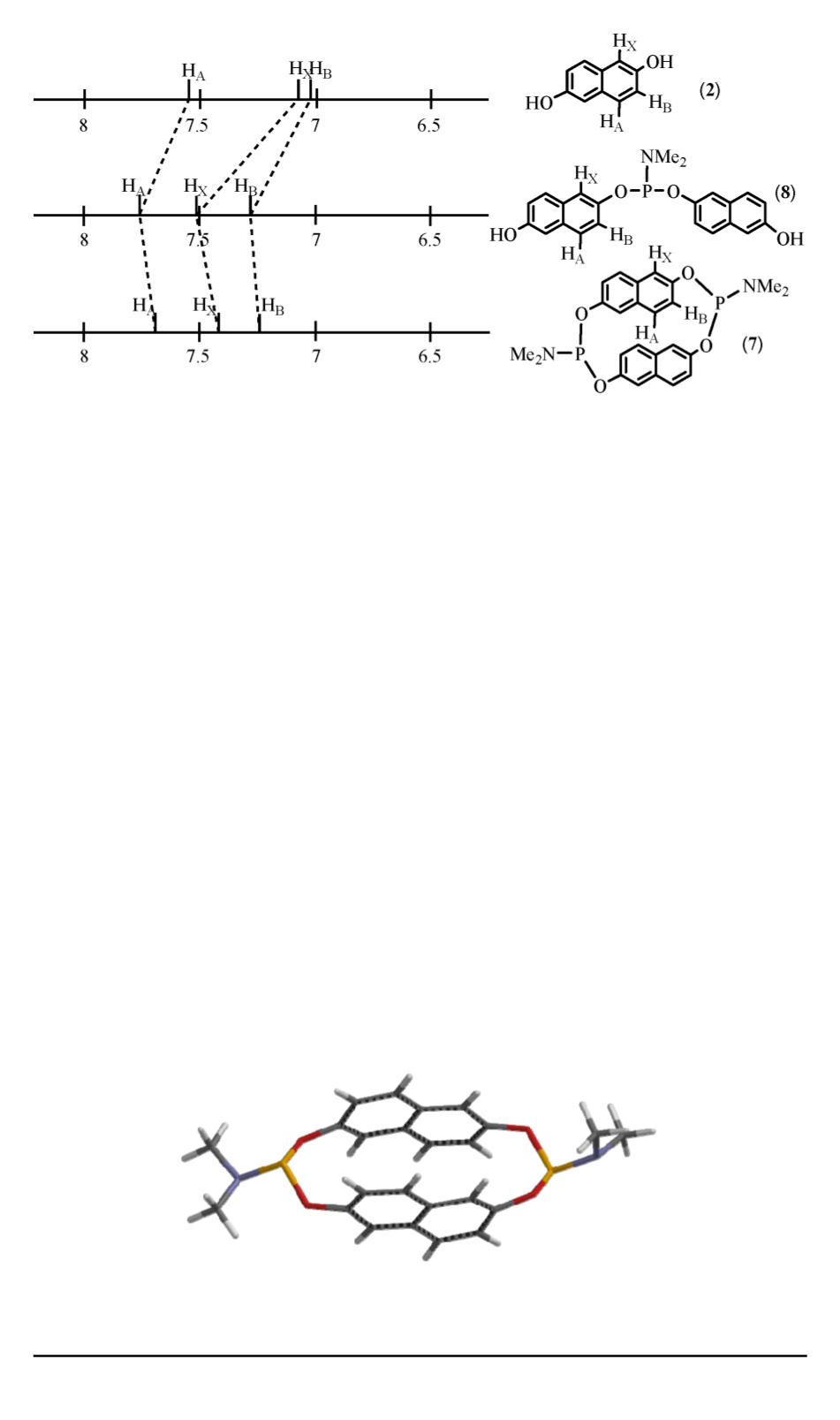
Рис. 4. Химические сдвиги (
δ
) ароматических АВХ-систем в соединениях 1, 6 и
5 (растворитель CDCl
3
, 400МГц)
Как и в случае с ациклическим производным 1,6-дигидроксинафта-
лина (6), за счет содержания электроноакцепторной амидофосфитной
группы у производного (8) наблюдается смещение сигналов аромати-
ческой части в слабое поле (7,78, 7,22 и 7,51 м.д. для протонов Н
А
, Н
В
и Н
Х
). Самое большое смещение будет у протона Н
Х
(
Δ
δ
= 0
,
55
м.д.).
При образовании циклической структуры (7) происходит смещение
всех сигналов (относительно ациклического производного (8)) в силь-
ное поле вследствие большей экранированности каждого нафталино-
вого кольца, что обусловлено их полным наложением друг на дру-
га. При этом смещение
Δ
δ
для всех протонов находится в пределах
0,1. . . 0,13 м.д. Значение КССВ Н
А
–Н
В
при переходе от соединения
(2) к ациклическому производному (8) и далее к нафтофосфациклофа-
ну (7) не изменяется (
Δ
J
≈
0
,
2
Гц).
Квантово-химические расчеты ab initio HF(3-21G) показали, что
для нафтофосфациклофана (7) наиболее энергетически выгодны кон-
формеры с полностью заслоненными нафталиновыми фрагментами
(7a) (рис. 5). Это согласуется с данными спектроскопии ЯМР
1
H. Уста-
новлено, что природа амидного заместителя у атома фосфора также
не влияет на взаимное расположение нафталиновых колец.
Рис. 5. Пространственное строение молекулы цикло[2,6-бис(нафтилендиметил-
амидофосфита)] (7), полученное по результатам компьютерного моделирования
100
ISSN 1812-3368. Вестник МГТУ им. Н.Э. Баумана. Сер. “Естественные науки”. 2014. № 1


